Es esencial para la vida, pero también es peligroso. No es combustible en sí mismo, pero facilita la combustión de otras cosas.
 |
| ANUSORN NAKDEE VIA GETTY IMAGES |
Por Manuel Peinado Lorca, catedrático. Departamento de Ciencias de la Vida e Investigador del Instituto Franklin de Estudios Norteamericanos, Universidad de Alcalá:
El oxígeno es el gas más abundante en la Tierra. Este elemento compone una quinta parte del aire y ocho de cada nueve partes del agua. Es esencial para la vida, pero también es peligroso. No es combustible en sí mismo, pero facilita la combustión de otras cosas. Menos mal, si no cada vez que encendiéramos una cerilla estallaría el aire que nos rodea.
La adecuada regulación del oxígeno en el organismo es una cuestión clave para el equilibrio fisiológico y para mantenernos vivos. Tanto, que su estudio ha valido más de un Premio Nobel.
Cuando respiramos tomamos oxígeno del aire, lo pasamos a los pulmones y de ahí, impulsado por un ventrículo, pasa primero por arterias y capilares hasta penetrar en las células. En las mitocondrias de su interior el oxígeno se incorpora al metabolismo celular.
En 1953, el bioquímico alemán Hans Adolf Krebs obtuvo el Premio Nobel de Fisiología o Medicina por unas elaboradísimas investigaciones que condujeron al conocido como ciclo de Krebs. Esta ruta metabólica está compuesta por una sucesión de reacciones químicas que forman parte de la respiración celular aerobia. Consiste en la liberación de la energía almacenada en carbohidratos, lípidos y proteínas para transformarla en energía química en forma de ATP (la moneda energética de intercambio celular). Como desecho, se libera dióxido de carbono.
La cantidad de oxígeno que llega hasta la matriz mitocondrial para producir energía debe ser la justa. Si reciben demasiado o muy poco, las mitocondrias no realizan bien su trabajo. El volumen ha de ser exactamente el adecuado, ni mayor ni menor, dentro de unos límites muy ajustados.
Por lo tanto, el cuerpo ha desarrollado una maquinaria molecular que ayuda a regular el oxígeno cuando los niveles ambientales son demasiado bajos o altos. Esto ocurre, por ejemplo, cuando el cuerpo se aclimata a altitudes más altas, lo que permite que las células se ajusten a los niveles más bajos de oxígeno.
Cómo se lleva a cabo esa regulación volumétrica o, si me permiten un símil, quién regula la llave de paso que el caudal de oxígeno que penetra en las células, ha sido el objetivo investigador de los tres científicos que han obtenido el Premio Nobel de Fisiología o Medicina 2019. A saber: el investigador del cáncer William Kaelin de la Universidad de Harvard, el médico Peter Ratcliffe de la Universidad de Oxford y el genetista Gregg Semenza de la Universidad Johns Hopkins.
Cáncer y anemia
El Nobel lo han recibido por describir cómo las células perciben y responden a los niveles cambiantes de oxígeno activando y desactivando genes. Este descubrimiento resulta clave para comprender enfermedades humanas como el cáncer y la anemia. Su trabajo ha ayudado a a comprender cómo el cuerpo se adapta a los bajos niveles de oxígeno, por ejemplo, produciendo glóbulos rojos y desarrollando nuevos vasos sanguíneos.
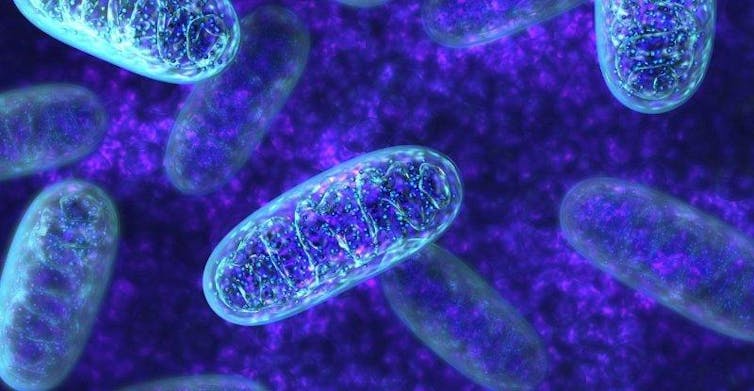 |
| as mitocondrias son los orgánulos encargados de producir energía dentro de la célula, algo así como el motor celular. Las mitocondrias cuentan con su propio genoma, el llamado ADN mitocondrial. |
Los tejidos del cuerpo pueden verse privados de oxígeno con la altitud, durante el ejercicio o cuando se interrumpe el flujo sanguíneo, como durante un derrame cerebral. La capacidad de las células para detectar oxígeno también es crucial para el crecimiento adecuado de un feto y de una placenta en desarrollo, y para el crecimiento importante de un tumor, porque la masa de células de crecimiento rápido puede agotar el oxígeno en el interior del mismo.
En los trabajos de investigación realizados en la década de 1990 que han sido premiados ahora, los tres científicos, trabajando independientemente, descubrieron los procesos moleculares que llevan a cabo las células para responder a los niveles de oxígeno en el cuerpo. El elemento central del control es un mecanismo que involucra a unas proteínas llamadas HIF y VHL.
Semenza y Ratcliffe estudiaron la regulación de una hormona llamada eritropoyetina (EPO), que, como pronto descubrieron los ciclistas, es crucial para estimular la producción de glóbulos rojos en respuesta a bajos niveles de oxígeno. Sin embargo, no se sabía cómo variaban los niveles de oxígeno que provocaban que los genes EPO se activaran.
Utilizando ratones modificados, Semenza y su equipo encontraron la respuesta: identificaron un par de genes que codifican dos proteínas que forman un complejo proteínico llamado factor inducible por hipoxia (HIF), que pueden unirse al ADN activando ciertos genes estimuladores de la producción de EPO cuando el nivel de oxígeno es bajo.
Mientras tanto, Kaelin estaba investigando en la enfermedad de von Hippel-Lindau, una enfermedad rara producida por mutaciones genéticas que aumentan dramáticamente el riesgo de algunos tipos de cáncer en las familias que la padecen. En concreto, los cánceres están asociados con la sobreproducción de vasos sanguíneos y una mayor producción de EPO. Kaelin demostró que un gen al que llamó VHL estaba involucrado en cómo las células responden al oxígeno.
Ratcliffe y su equipo descubrieron más tarde que la proteína expresada por el gen VHL interactúa con uno de los componentes del HIF, desactivando las respuestas a condiciones de bajo oxígeno al marcar el componente HIF para que se inhiba una vez que los niveles de oxígeno aumentan.
En 2001, los equipos liderados por Kaelin y Ratcliffe demostraron que, como parte de este proceso, una modificación química de la proteína VHL, llamada prolil-hidroxilación, permite que las células respondan increíblemente rápido a los niveles de oxígeno. En presencia de oxígeno, la forma modificada de VHL puede unirse al HIF, lo que conduce a su inhibición. Pero esta modificación se bloquea cuando las células carecen de oxígeno, lo que inicia la actividad del HIF. Era un mecanismo tan simple como eficaz: las células pueden reaccionar en minutos a los bajos niveles de oxígeno simplemente bloqueando la inhibición del HIF.
La investigación no solo aporta conocimiento sobre el proceso bioquímico de detección de oxígeno, sino que también abre nuevas vías para combatir enfermedades comunes. En la insuficiencia renal crónica, por ejemplo, la expresión reducida de EPO a menudo produce anemia. Muchos cánceres estimulan el sistema de detección de oxígeno para estimular el crecimiento de los vasos sanguíneos y crear las condiciones adecuadas para la propagación de las células cancerosas.
Actualmente se están realizando investigaciones para desarrollar medicamentos que puedan activar o bloquear estos sensores de oxígeno para combatir estas enfermedades. También se están investigando los medicamentos inhibidores de la prolil-hidroxilasa que eviten que el VHL se una al HIF y provoque su inhibición, como tratamientos para la anemia y la insuficiencia renal.


No hay comentarios:
Publicar un comentario